Смешанная гиперлипидемия характеризуется повышенным уровнем липопротеинов низкой плотности (ЛПНП) и липопротеинов, богатых триглицеридами, в плазме, что приводит к повышенному риску развития атеросклеротических сердечно-сосудистых заболеваний у этой группы пациентов.
ANGPTL3 ингибирует липопротеинлипазу и эндосепиазу, а также поглощение печенью липопротеинов, богатых триглицеридами. У носителей инактивированного варианта ANGPTL3 наблюдались более низкие уровни триглицеридов, холестерина ЛПНП, холестерина липопротеинов высокой плотности (ЛПВП) и не-ЛПВП, а также более низкий риск атеросклеротических сердечно-сосудистых заболеваний. Зодасиран — это препарат на основе малой интерферирующей РНК (РНК-интерференции), направленный на экспрессию ANGPTL3 в печени.
Смешанная гиперлипидемия характеризуется повышенным уровнем холестерина липопротеинов низкой плотности (ЛПНП) и липопротеинов, богатых триглицеридами. Липопротеины, богатые триглицеридами (включая хиломикроны, липопротеины очень низкой плотности (ЛПОНП) и остаточный холестерин), играют важную роль в развитии атеросклеротического заболевания. Эффективного лечения смешанной гиперлипидемии не существует.
Известно, что Бейтс снижает уровень триглицеридов (ТГ), но это снижение ограничено. В то же время препараты, снижающие уровень ТГ, включая Бейтс (например, эйкозапентаеновая уксусная кислота и др.), не оказывают существенного влияния на риск атеросклеротического поражения, вызванного повышенным уровнем остаточного холестерина. Кроме того, предыдущие исследования с участием пациентов, уже принимающих статины, показали, что комбинированные препараты, снижающие уровень ТГ, не снижают риск сердечно-сосудистых событий. Эти факторы существенно затрудняют лечение смешанной гиперлипидемии.
ANGPTL3 (ангиопоэтин-подобный белок 3) регулирует метаболизм липидов и липопротеинов, включая ТГ и холестерин липопротеинов невысокой плотности (ЛПВП), обратимо ингибируя липопротеинлипазу, эндосепиазу и рецептор-зависимый захват липопротеинов низкой плотности (ЛПНП) печенью. Было обнаружено, что вариант инактивации ANGPTL3 приводит к повышению активности липопротеинлипазы и эндосепиазы, что, в свою очередь, в большинстве случаев приводит к снижению уровня липопротеинов в плазме. К ним относятся липопротеины, богатые триглицеридами (т. е. хиломикроны, остаточный холестерин, ЛПОНП, липопротеины средней плотности [ЛПСП]), ЛПНП, липопротеины высокой плотности (ЛПВП), липопротеин (а) и их холестериновые компоненты. У гетерозиготных носителей этого варианта риск атеросклеротического заболевания снижен примерно на 40%, при этом неблагоприятных клинических проявлений не выявлено. ANGPTL3 экспрессируется в печени, и методы терапии подавления генов, направленные на его мРНК, известные как препараты малых интерферирующих РНК (siRNA), являются перспективным гибридным методом лечения гиперлипидемии.
12 сентября 2024 года в журнале New England Journal of Medicine (NEJM) было опубликовано исследование ARCHES 2, подтверждающее, что препарат siRNA зодасиран значительно снизил уровень ТГ у пациентов со смешанной гиперлипидемией [1]. ARCHES-2 — это двойное слепое плацебо-контролируемое исследование фазы 2b с широким диапазоном доз. В исследование было включено 204 пациента со смешанной гиперлипидемией (уровень ТГ натощак 150–499 мг/дл, уровень ХС ЛПНП ≥70 мг/дл или уровень не-ХС ЛПВП ≥100 мг/дл). Пациенты были разделены на группы зодасирана 50 мг, 100 мг, 200 мг и контрольную группу плацебо. Пациенты получали подкожные инъекции на 1-й и 12-й неделе и получали последующую профилактику до 36-й недели.
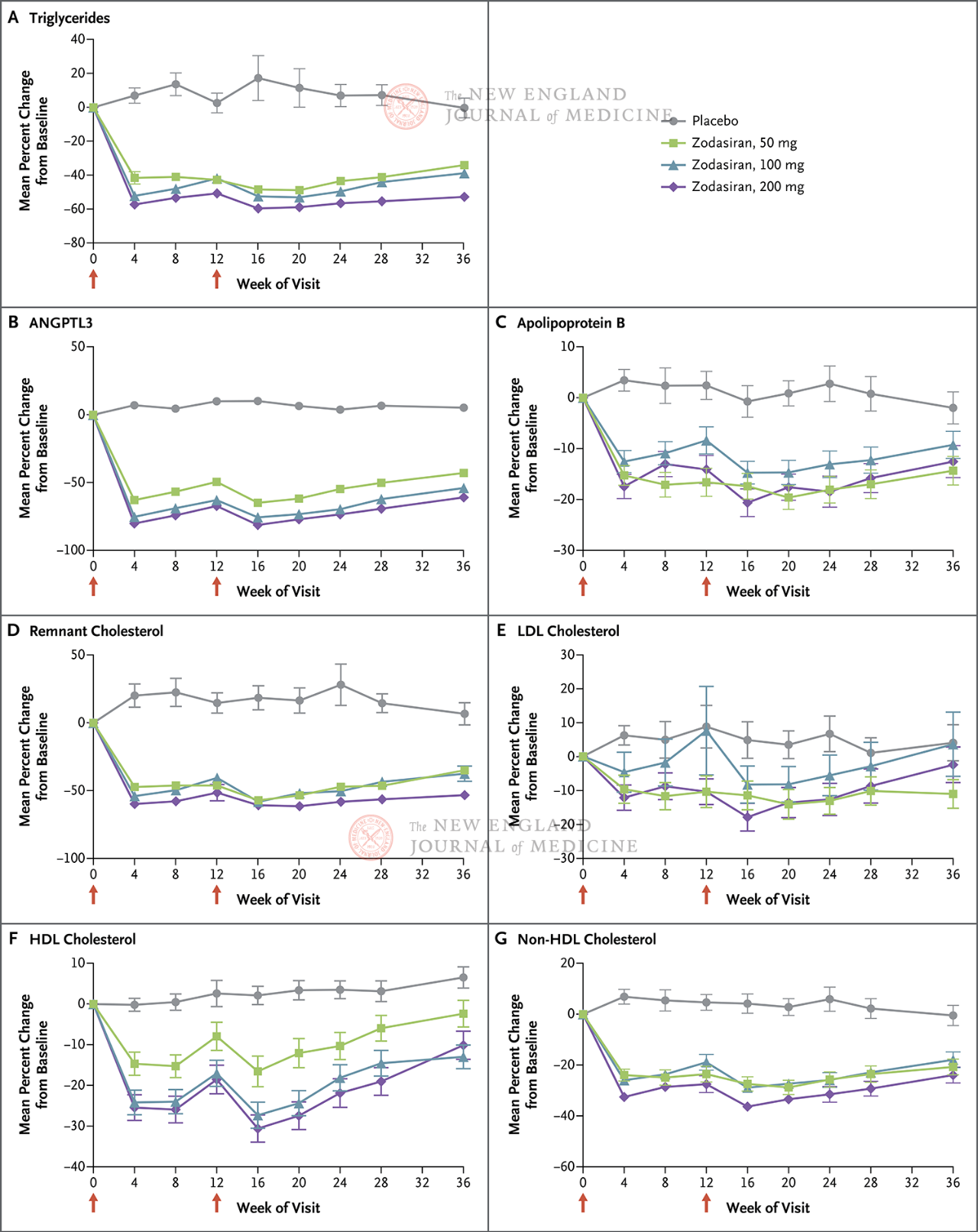
Первичной конечной точкой было процентное изменение ТГ от исходного уровня к 24-й неделе. Исследование показало, что к 24-й неделе уровни ТГ в группе зодасирана значительно снизились дозозависимым образом (уровни ТГ в каждой группе дозировки снизились на 51, 57 и 63 процентных пункта соответственно по сравнению с группой плацебо) (P < 0,001 для всех сравнений). ANGPTL3 также снизился на 54, 70 и 74 процентных пункта соответственно. Уровни не-ЛПВП снизились на 29, 29 и 36 процентных пунктов, уровни аполипопротеина B снизились на 19, 15 и 22 процентных пункта, а уровни ЛПНП снизились на 16, 14 и 20 процентных пунктов соответственно, и эти результаты сохранялись до 36-й недели. На 24-й неделе зодасиран
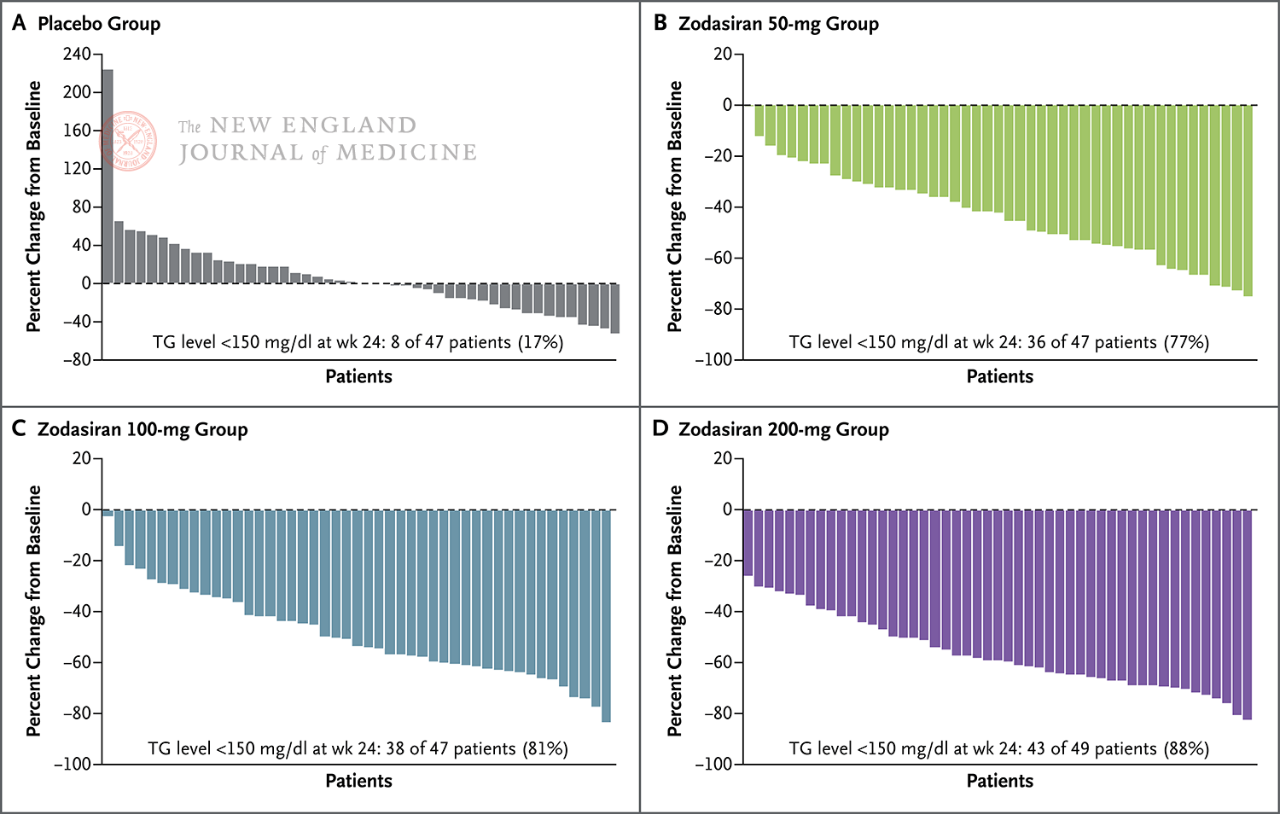
У 88% пациентов в группе 200 мг уровень ТГ натощак снизился до нормального уровня.
Красные стрелки на 1-й и 12-й дни указывают на введение зодасирана или плацебо.
Уровень ТГ натощак снизился до нормы на 24-й неделе (150
мг/дл или меньше)
Каждый столб представляет одного пациента.
Исследование также показало безопасность зотасирана во всех группах дозирования, и только 2 пациента прекратили исследование из-за нежелательных явлений (1 в группе плацебо и 1 в группе зотасирана 100 мг). Все серьёзные нежелательные явления в группе зотасирана исчезли к концу исследования, в группе плацебо зафиксирован один летальный исход. Единственным нежелательным явлением, вызывающим беспокойство, было повышение уровня HBA1c в группе зотасирана 200 мг по сравнению с плацебо (среднее изменение от исходного уровня к 24-й неделе [±SD] 0,38 ± 0,66% против -0,03 ± 0,88% у пациентов с уже имеющимся диабетом). Пациенты без диабета составили 0,12 ± 0,19% против -0,03 ± 0,19%.
В частности, почти все пациенты в исследовании (96%) принимали статины (из которых 37% — высокие дозы), 1% — ингибитор пропротеинпревращающего фермента субтилизин 9 (PCSK9i), а 21% — фибраты. Таким образом, добавление зодасирана к существующей стандартной схеме лечения по-прежнему обеспечивало значительный гиполипидемический эффект, что открывает новые возможности для лечения смешанной гиперлипидемии в будущем.
На 24-й неделе максимальная доза зотасирана 200 мг в исследовании снизила уровень остаточного холестерина на 34,4 мг/дл по сравнению с плацебо. Согласно текущим моделям, ожидается, что это снижение приведет к снижению частоты серьезных сердечных осложнений на 20%. Зодасиран потенциально может использоваться в качестве монотерапии всеми липопротеиновыми компонентами для снижения риска сердечно-сосудистых событий у пациентов. Поэтому необходимы дальнейшие исследования для определения потенциала этого препарата в снижении риска атеросклеротического поражения.
В двойном слепом рандомизированном плацебо-контролируемом исследовании MUIR фазы 2b, опубликованном одновременно в NEJM, для лечения смешанной гиперлипидемии использовался другой препарат siRNA, плозасиран [2]. Плозасиран предназначен для снижения экспрессии APOC3, гена, кодирующего аполипопротеин C3 (APOC3), регулятора метаболизма ТГ, в печени, тем самым снижая уровни ТГ и остаточного холестерина. Снижение уровней ТГ и остаточного холестерина, наблюдавшееся в исследовании, было аналогично таковому, полученному в исследовании ARCHES-2. Поэтому предполагается, что у пациентов со смешанной гиперлипидемией два препарата оказывают схожее действие на снижение уровня липопротеинов, богатых триглицеридами, и остаточного холестерина.
Результаты двух исследований siRNA показывают, что это очень перспективный класс препаратов, который откроет новые возможности для лечения смешанной гиперлипидемии и улучшит сердечно-сосудистые исходы у пациентов.
Время публикации: 15 сентября 2024 г.