Нозокомиальная пневмония — самая распространённая и серьёзная внутрибольничная инфекция, из которых 40% приходится на вентилятор-ассоциированную пневмонию (ВАП). ВАП, вызванная рефрактерными возбудителями, по-прежнему представляет собой сложную клиническую проблему. В течение многих лет руководства рекомендовали ряд мер (таких как целенаправленная седация, приподнятое положение головы) для профилактики ВАП, однако ВАП развивается у 40% пациентов с интубацией трахеи, что приводит к более длительному пребыванию в больнице, более частому применению антибиотиков и даже к летальному исходу. Люди постоянно ищут более эффективные профилактические меры.
Вентилятор-ассоциированная пневмония (ВАП) – это новое заболевание, которое развивается через 48 часов после интубации трахеи и является наиболее распространённой и смертельно опасной внутрибольничной инфекцией в отделении интенсивной терапии (ОИТ). В рекомендациях Американского общества инфекционных заболеваний (2016 г.) ВАП разграничивается с определением внутрибольничной пневмонии (ВБП) (ВБП относится только к пневмонии, возникающей после госпитализации без интубационной трубки и не связанной с искусственной вентиляцией лёгких; ВАП – это пневмония после интубации трахеи и искусственной вентиляции лёгких), а Европейское общество и Китай считают ВАП по-прежнему особым типом ВБП [1-3].
У пациентов, получающих искусственную вентиляцию легких, заболеваемость ВАП колеблется от 9% до 27%, уровень смертности оценивается в 13%, и это может привести к увеличению системного использования антибиотиков, более длительной искусственной вентиляции легких, более длительному пребыванию в отделении интенсивной терапии и увеличению расходов [4-6]. ГП/ВАП у пациентов без иммунодефицита обычно вызывается бактериальной инфекцией, а распределение распространенных патогенов и характеристики их резистентности варьируются в зависимости от региона, класса больницы, популяции пациентов и воздействия антибиотиков, а также меняются с течением времени. Pseudomonas aeruginosa доминировала среди патогенов, связанных с ВАП, в Европе и Америке, в то время как больше Acinetobacter baumannii было выделено в третичных больницах Китая. От одной трети до половины всех смертей, связанных с ВАП, напрямую вызваны инфекцией, при этом уровень смертности в случаях, вызванных Pseudomonas aeruginosa и ацинетобактером, был выше [7,8].
В связи с сильной гетерогенностью ВАП диагностическая специфичность клинических проявлений, методов визуализации и лабораторных исследований низкая, а спектр дифференциальной диагностики широк, что затрудняет своевременную диагностику ВАП. В то же время, бактериальная резистентность представляет собой серьезную проблему для лечения ВАП. По оценкам, риск развития ВАП составляет 3% в день в течение первых 5 дней использования искусственной вентиляции легких, 2% в день между 5 и 10 днями и 1% в день в остальное время. Пик заболеваемости обычно приходится на 7 дней вентиляции легких, поэтому существует окно, в течение которого инфекцию можно предотвратить на ранней стадии [9,10]. Многие исследования посвящены профилактике ВАП, но, несмотря на десятилетия исследований и попыток профилактики ВАП (таких как избегание интубации, предотвращение повторной интубации, снижение седации, подъем изголовья кровати на 30–45° и уход за полостью рта), заболеваемость, по-видимому, не снизилась, а связанная с этим медицинская нагрузка остается очень высокой.
Ингаляционные антибиотики используются для лечения хронических инфекций дыхательных путей с 1940-х годов. Поскольку они могут максимизировать доставку лекарств к целевому месту инфекции (т. е. дыхательным путям) и снизить системные побочные эффекты, они показали хорошую ценность для применения при различных заболеваниях. Ингаляционные антибиотики в настоящее время одобрены Управлением по контролю за продуктами и лекарствами США (FDA) и Европейским агентством по лекарственным средствам (EMA) для использования при муковисцидозе. Ингаляционные антибиотики могут значительно снизить бактериальную нагрузку и частоту обострений при бронхоэктатической болезни без увеличения общих побочных эффектов, и текущие руководящие принципы признали их в качестве терапии первой линии для пациентов с инфекцией синегнойной палочки и частыми обострениями; ингаляционные антибиотики в периоперационный период трансплантации легких также могут использоваться в качестве адъювантных или профилактических препаратов [11,12]. Однако в рекомендациях США по лечению ВАП 2016 года эксперты не были уверены в эффективности адъювантных ингаляционных антибиотиков из-за отсутствия крупных рандомизированных контролируемых исследований. Исследование фазы 3 (INHALE), опубликованное в 2020 году, также не дало положительных результатов (ингаляционное введение амикацина в сочетании с внутривенным введением антибиотиков при грамотрицательной бактериальной инфекции, вызванной пациентами с ВАП; двойное слепое, рандомизированное, плацебо-контролируемое исследование эффективности фазы 3; в общей сложности 807 пациентов; системное лечение + вспомогательная ингаляция амикацина в течение 10 дней).
В этом контексте группа исследователей под руководством исследователей из Регионального университетского клинического центра Тура (CHRU) во Франции приняла иную исследовательскую стратегию и провела многоцентровое двойное слепое рандомизированное контролируемое исследование эффективности (AMIKINHAL), инициированное исследователем. Сравнение эффективности ингаляционного амикацина и плацебо для профилактики ВАП проводилось в 19 отделениях интенсивной терапии во Франции [13].
В общей сложности 847 взрослых пациентов, которым проводилась инвазивная искусственная вентиляция лёгких в течение 72–96 часов, были рандомизированы в соотношении 1:1 к ингаляциям амикацина (N= 417, 20 мг/кг идеальной массы тела, 1 раз в день) или ингаляциям плацебо (N=430, 0,9% эквивалент хлорида натрия) в течение 3 дней. Первичной конечной точкой был первый эпизод ВАП с начала рандомизации до 28-го дня.
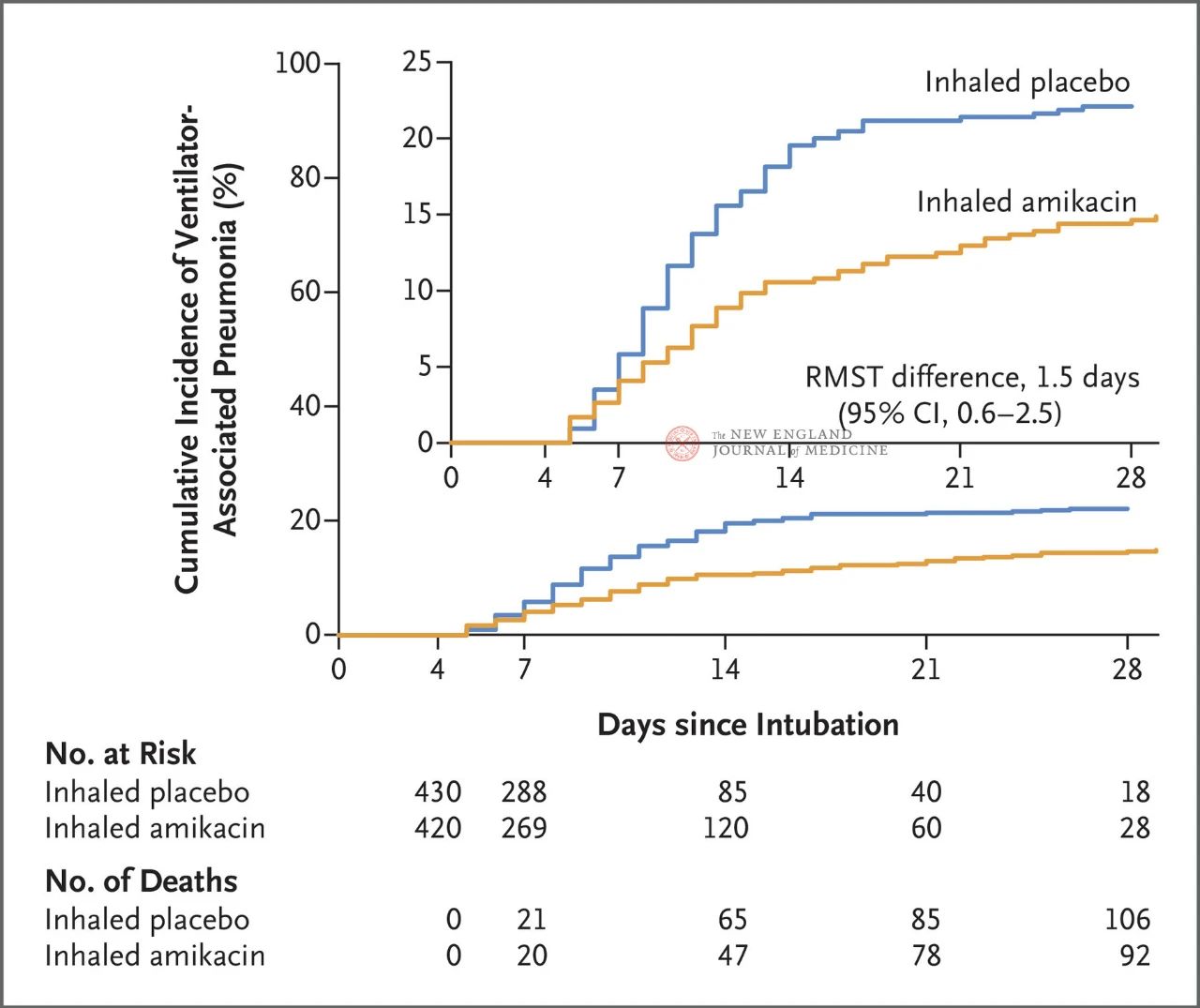
Результаты исследования показали, что через 28 дней у 62 пациентов (15%) в группе амикацина развилась ВАП, а у 95 пациентов (22%) в группе плацебо развилась ВАП (ограниченная средняя разница в выживаемости для ВАП составила 1,5 дня; 95% ДИ, 0,6–2,5; P=0,004).
Что касается безопасности, то у семи пациентов (1,7%) в группе амикацина и четырёх пациентов (0,9%) в группе плацебо наблюдались серьёзные нежелательные явления, связанные с исследованием. Среди тех, у кого не было острого повреждения почек на момент рандомизации, у 11 пациентов (4%) в группе амикацина и у 24 пациентов (8%) в группе плацебо острое повреждение почек наблюдалось на 28-й день (ОР 0,47; 95% ДИ 0,23–0,96).
Клиническое исследование имело три важных момента. Во-первых, с точки зрения дизайна исследования, исследование AMIKINHAL основано на исследовании IASIS (рандомизированном двойном слепом плацебо-контролируемом параллельном исследовании 2 фазы с участием 143 пациентов). Для оценки безопасности и эффективности системного лечения грамотрицательной бактериальной инфекции, вызванной ВАП, ингаляционным методом амикацина и фосфомицином (INHALE) и завершения исследования с отрицательными результатами был сделан вывод о том, что, фокусируясь на профилактике ВАП, были получены относительно хорошие результаты. Учитывая высокую смертность и длительную госпитализацию пациентов с искусственной вентиляцией легких и ВАП, если ингаляция амикацина может обеспечить существенно различающиеся результаты в снижении смертности и продолжительности госпитализации у этих пациентов, это будет иметь большую ценность для клинической практики. Однако, учитывая неоднородность позднего лечения и ухода у каждого пациента и в каждом центре, существует ряд сопутствующих факторов, которые могут помешать проведению исследования, поэтому получение положительного результата, связанного с ингаляционными антибиотиками, может быть затруднено. Таким образом, для успешного клинического исследования необходим не только превосходный дизайн исследования, но и выбор соответствующих первичных конечных точек.
Во-вторых, хотя аминогликозидные антибиотики не рекомендуются в качестве единственного препарата в различных руководствах по лечению ВАП, они могут охватывать распространённые патогены у пациентов с ВАП (включая синегнойную палочку, ацинетобактер и т. д.) благодаря своей ограниченной абсорбции в эпителиальных клетках лёгких, высокой концентрации в месте инфекции и низкой системной токсичности. Аминогликозидные антибиотики широко распространены среди ингаляционных антибиотиков. Данная статья согласуется с комплексной оценкой размера эффекта интратрахеального введения гентамицина в небольших выборках, опубликованной ранее, которая в совокупности демонстрирует эффективность ингаляционных аминогликозидных антибиотиков в профилактике ВАП. Следует также отметить, что большинство плацебо-контролей, выбранных в исследованиях, связанных с ингаляционными антибиотиками, представляли собой физиологический раствор. Однако, учитывая, что распыляемая ингаляция физиологического раствора сама по себе может играть определенную роль в разжижении мокроты и содействии отхаркиванию, физиологический раствор может вызывать определенные помехи при анализе результатов исследования, что следует всесторонне учитывать в ходе исследования.
Кроме того, важна локальная адаптация лечения HAP/VAP, а также антибиотикопрофилактика. В то же время, независимо от продолжительности интубации, экология местного отделения интенсивной терапии является наиболее важным фактором риска инфицирования полирезистентными бактериями. Поэтому эмпирическое лечение должно максимально опираться на микробиологические данные местных больниц и не может слепо ссылаться на руководства или опыт больниц третьего уровня. В то же время, у пациентов в критическом состоянии, которым требуется искусственная вентиляция легких, часто сочетаются полисистемные заболевания, и под совокупным действием множества факторов, таких как стрессовое состояние, также может наблюдаться явление перекрестного проникновения кишечных микробов в легкие. Высокая гетерогенность заболеваний, вызванных внутренней и внешней суперпозицией, также определяет, что широкомасштабное клиническое продвижение каждого нового вмешательства - это долгий путь.
Время публикации: 02.12.2023